1998.7.18 I.Takagi
1998.7.31 rev.1
(概要)
固体元素の定積モル比熱が、常温付近ではどれもほとんど等しく、3R (Rは気体定数)であるという法則。Dulong も Petit もフランスの科学者で、1819年に発表した。
(説明)
固体の原子が結晶格子の位置に規則的に並んでおり、各原子はその位置の周りで小さな振動運動をしているとする。簡単のため、質量mの原子が1次元の単振動をしている(質量mの調和振動子)と考えると、そのエネルギーは運動エネルギー(p2/2m) とポテンシャルエネルギー(αx2/2) の和である。ここで、p は運動量、αはバネ定数で、xは変位量である。古典統計力学の近似が成り立つとすれば、等分配則(注1)によって、各エネルギーの平均値は kT/2 に等しいから、両者の和は kTとなる (kとT はそれぞれボルツマン定数と絶対温度である)。
実際の結晶中では、原子は格子位置の周りで3次元的な単振動を行っていると考えられるから、全エネルギーは 3kTとなる。従って、1モルの原子を含む固体の平均エネルギーEは、3RTとなる(注2)。 定積モル比熱Cvは、体積一定のもとでEをTで偏微分することによって得られるから、
Cv = (∂E/∂T)V = 3R (1)
となる。
(具体例とコメント)
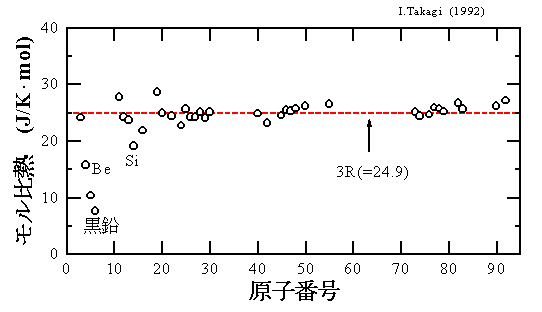
下図にいくつかの元素の 0゚C における定圧モル比熱(注3)を示す。大部分の元素については 3R という値に極めてよく一致していることがわかるであろう。黒鉛やSi等にとっては、0゚C は古典的とみなせるほど高い温度ではない(注4)ために 3R から外れてしまったと考えられる。
古典的に考えると、金属中では、自由電子があたかも気体のように振る舞っている。原子1個当たり1個程度の自由電子が存在するだろうから、自由電子によるモル比熱は 3R/2 となり、上述した格子振動による比熱と併せると、9R/2 になってしまう。実際には自由電子は古典的に考えることはできず(注4)、自由電子に分配されるエネルギーの平均値は 3kT/2 よりも極めて小さいため、Dulong-Petit の法則は金属においても充分よい近似で成り立っている。
(注1)古典統計力学において、ある系が温度Tで熱平衡にあるとき、系のエネルギーのうち、独立な二次の項は、それぞれ kT/2 に等しい平均値を持つという法則。調和振動子の場合、運動エネルギーにおける p2 とポテンシャルエネルギーにおける x2 が、「独立な二次」に該当する。 (注2)アボガドロ数を N とすると、R = kN であるから。 (注3)理論的に扱われるのが定積比熱であるのに対し、測定されるのは定圧比熱であるが、固体の場合、両者に差は無いと考えても差し支えない。 (注4)古典的に考えてよいかどうかは不確定性原理から判断することができる。これについては後日記述してリンクするかもしれない。(追記) 1998.7.25 に補足記事を作成した。

以上
このページは、高木郁二が担当している京都大学工学部物理工学科の講義・実験を補う資料として作成したものです。ご意見・お問い合わせはこちらまでお願いします。